您现在的位置:首页>类风湿性关节炎
-
+ 全部展开 -全部收缩
-
-概述
疾病概述:类风湿关节炎(rheumatoid arthritis,RA)是以侵蚀性、对称性多关节炎为主要临床表现的慢性、全身性自身免疫性疾病。确切发病机制不明。基本病理改变为滑膜炎、血管翳形成,并逐渐出现关节软骨和骨破坏,最终可能导致关节畸形和功能丧失。早期诊断、早期治疗至关重要。本病呈全球性分布,是造成人类丧失劳动力和致残的主要原因之一。我国RA的患病率0.32%~0.36%左右。
- -预防
-
+流行病学
流行病学:流行病学调查显示,RA 的全球发病率为 0.5%~1%,中国大陆地区发病率为 0.42%,总患病人群约 500万,男女患病比率约为1∶4。我国RA患者在病程1~5年、5~10 年、10~15 年及≥15 年的致残率分别为 18.6%、43.5%、48.1%、61.3%,随着病程的延长,残疾及功能受限发生率升高。RA不仅造成患者身体机能、生活质量和社会参与度下降,也给患者家庭和社会带来巨大的经济负担。
-
+病因
-
+发病机制
发病机制:1.关节病变(1)滑膜的改变:关节病变由滑膜开始,滑膜充血、水肿。以靠近软骨边缘的滑膜最为明显。在滑膜表面有纤维蛋白渗出物覆盖。 滑膜有淋巴细胞、浆细胞及少量多核粒细胞浸润。在滑膜下层浸润的细胞,形成“淋巴样小结”,有些在小血管周围聚集。滑膜表层细胞增生呈栅栏状,表面绒毛增生。在晚期大部分浸润细胞为浆细胞,关节腔内有渗出液。(2)肉芽肿形成:在急性炎症消退后,渗出波逐步吸收。在细胞浸润处毛细血管周围成纤维细胞增生明显。滑膜细胞成柱状,呈栅栏状排列,滑膜明显增厚呈绒毛状。滑膜内血管增生,滑膜内血管增多,即成肉芽肿,并与软骨粘连,向软骨内侵入。 血管内膜细胞中有溶酶体空泡形成;血管周围有浆细胞围绕,滑膜内并可见“类风湿细胞”聚集。(3)关节软骨及软骨下骨的改变:由于由滑膜出现的肉芽组织血管导向软骨内覆盖侵入,逐渐向软骨中心部位蔓延, 阻断了软骨由滑液中吸收营养,软骨逐步被吸收。同时由于溶酶体内的蛋白降解酶、胶原酶的释放,使软骨基质破坏、溶解,导致关节软骨广泛破坏,关节间隙变窄,关节面粗糙不平,血管翳机化后形成粘连,纤维组织增生,关节腔内形成广泛粘连, 而使关节功能明显受限,形成纤维性强直。待关节软骨面大部吸收后,软骨下骨大面积破骨与成长反应同时发生,在骨端间形成新骨,而致关节骨性强直。由于关节内长期反复积液,致关节囊及其周围韧带受到牵拉而延长松弛。 再加上关节面和骨端的破坏,使关节间隙变窄,使关节韧带更为松弛。由于关节炎症及软骨面破坏,病人因疼痛常处于强迫体位。关节周围的肌肉发生保护性痉挛。关节周围的肌肉、肌腱、韧带和筋膜也受到病变侵犯而粘连,甚至断裂,最后导致关节脱位或畸形位骨性强直。2.关节外表现(1)类风湿性皮下结节:类风湿性皮下结节是诊断类风湿的可靠证据,结节是肉芽肿改变,其中心坏死区含有IgG和RF免疫复合物。周围为纤维细胞、淋巴细胞 及单核细胞所包围,最后变为致密的结缔组织。(2)肌腱及腱鞘、滑囊炎症:肌腱及腱鞘炎在手足中常见,肌腱和鞘膜有淋巴细胞、单核细胞、浆细胞浸润。严重者可触及腱上的结节,肌腱可断裂及粘连,是导致周围关节畸形的原因。 滑囊炎以跟腱滑囊炎多见,在肌腱附着处常形成局限性滑膜炎,甚至可引起局部骨质增生或缺损。滑囊炎也可能发生在腘窝部位,形成腘窝囊肿。
-
+临床表现
临床表现:流行病学资料显示,RA发生于任何年龄,80%发病于35~50岁,女性患者约3倍于男性。RA的临床个体差异大,从短暂、轻微的少关节炎到急剧、进行性多关节炎及全身性血管炎表现均可出现,常伴有晨僵。RA多以缓慢隐匿的方式起病,在出现明显关节症状前可有数周的低热,少数患者可有高热、乏力、全身不适、体重下降等症状,以后逐渐出现典型关节症状。少数则急剧起病,在数天内出现多个关节症状。可分滑膜炎症状和关节结构破坏的表现,前者经治疗后有一定可逆性,但后者一经出现很难逆转。RA病情和病程有个体差异,从短暂、轻微的少关节炎到急剧进行性多关节炎,常伴有晨僵。早晨起床后关节及其周围僵硬感,称“晨僵”(morning stiffness)。持续时间超过1小时者意义较大。晨僵出现在95%以上的RA患者。它常被作为观察本病活动的指标之一,只是主观性很强。其他病因的关节炎也可出现晨僵,但不如本病明显和持久。关节痛往往是最早的症状,最常出现的部位为腕、掌指、近端指间关节,其次是足趾、膝、踝、肘、肩等关节。多呈对称性、持续性,但时轻时重,疼痛的关节往往伴有压痛,受累关节的皮肤可出现褐色色素沉着。多因关节腔内积液或关节周围软组织炎症引起,病程较长者可因滑膜慢性炎症后的肥厚而引起肿胀。凡受累的关节均可肿胀,常见的部位与关节痛部位相同,亦多呈对称性。见于较晚期患者,关节周围肌肉的萎缩、痉挛则使畸形更为加重。最为常见的关节畸形是腕和肘关节强直、掌指关节的半脱位、手指向尺侧偏斜和呈“天鹅颈(swan neck)”样及“纽扣花样(boutonniere)”表现。重症患者关节呈纤维性或骨性强直失去关节功能,致使生活不能自理。(1)颈椎的可动小关节及周围腱鞘受累出现颈痛、活动受限,有时甚至因颈椎半脱位而出现脊髓受压。(2)肩、髋关节:其周围有较多肌腱等软组织包围,因此很难发现肿。最常见的症状是局部痛和活动受限,髋关节往往表现为臀部及下腰部疼痛。(3)颞颌关节:出现于1/4的RA患者,早期表现为讲话或咀嚼时疼痛加重,严重者有张口受限。关节肿痛和结构破坏都引起关节的活动障碍。美国风湿病学会将因本病而影响生活的程度分为四级:Ⅰ级:能照常进行日常生活和各项工作;Ⅱ级:可进行一般的日常生活和某种职业工作,但参与其他项目活动受限;Ⅲ级:可进行一般的日常生活,但参与某种职业工作或其他项目活动受限;Ⅳ级:日常生活的自理和参与工作的能力均受限。是本病较常见的关节外表现,可见于20%~30%的患者,多位于关节隆突部及受压部位的皮下,如前臂伸面、肘鹰嘴突附近、枕、跟腱等处。其大小不一,结节直径由数毫米至数厘米,质硬、无压痛,对称性分布。此外,几乎所有脏器如心、肺、眼等均可累及。其存在提示有本病的活动。RA患者系统性血管炎少见,体格检查能观察到的有指甲下或指端出现的小血管炎,少数引起局部组织的缺血性坏死。眼受累多为巩膜炎,严重者因巩膜软化而影响视力。RF阳性的患者可出现亚临床型的血管炎,如无临床表现的皮肤和唇腺活检可有血管壁免疫物质的沉积,亚临床型血管炎的长期预后尚不明确。肺受累很常见,其中男性多于女性,有时可为首发症状。(1) 肺间质病变:是最常见的肺病变,见于约30%的患者,主要表现为活动后气短,肺纤维化,肺功能和肺影像学如肺部高分辨CT有助于早期诊断。(2) 结节样改变:肺内出现单个或多个结节,为肺内的类风湿结节表现。结节有时可液化,咳出后形成空洞。(3) Caplan综合征:尘肺患者合并RA时易出现大量肺结节,称之为Caplan综合征,也称类风湿性尘肺病。临床和胸部X线表现均类似肺内的类风湿结节,数量多,较大,可突然出现并伴关节症状加重。病理检查结节中心坏死区内含有粉尘。(4)胸膜炎:见于约10%的患者。为单侧或双侧性的少量胸腔积液,偶为大量胸腔积液。胸水呈渗出性,糖含量很低。(5)肺动脉高压:一部分是肺内动脉病变所致的肺动脉高压,另一部分为肺间质病变引起的肺动脉高压。RA患者可以出现心脏受累,心包炎最常见,多见于RF阳性、有类风湿结节的患者,但多数患者无相关临床表现。通过超声心动图检查约30%的患者出现小量心包积液。患者可有上腹不适、胃痛、恶心、纳差、甚至黑粪,多与服用抗风湿药物,尤其是非甾体抗炎药有关,很少由RA本身引起。本病的血管炎很少累及肾,偶有轻微膜性肾病、肾小球肾炎、肾内小血管炎以及肾脏的淀粉样变等报道。神经受压是RA患者出现神经系统病变的常见原因。如正中神经在腕关节处受压可出现腕管综合征。多数患者随着炎症减轻神经症状能逐渐好转,但有时需要手术减压治疗。脊髓受压表现为渐起的双手感觉异常和力量的减弱,腱反射多亢进,病理反射阳性。多发性单神经炎则因小血管炎的缺血性病变所造成。患者的贫血程度通常和病情活动度相关,尤其是和关节的炎症程度相关。RA患者的贫血一般是正细胞正色素性贫血,本病出现小细胞低色素性贫血时,贫血可因病变本身或因服用非甾体抗炎药而造成胃肠道长期少量出血所致;此外,与慢性疾病性贫血的发病机制有关,在患者的炎症得以控制后,贫血也可得以改善。在病情活动的RA患者常见血小板增多,与疾病活动度相关,病情缓解后可下降。Felty综合征是指RA患者伴有脾大、中性粒细胞减少,有的甚至有贫血和血小板减少。RA患者出现Felty综合征时并非都处于关节炎活动期,其中很多患者合并有下肢溃疡、色素沉着,皮下结节,关节畸形,以及发热、乏力、食欲减退和体重下降等全身表现。部分患者常有口干、眼干症状,30%~40%的RA患者可继发干燥综合征,需结合自身抗体,经口腔科及眼科检查进一步明确诊断。
-
+并发症
并发症:病情严重者,可出现畸形位骨性强直,甚至关节脱位。
-
+实验室检查
实验室检查:有轻至中度贫血。活动期患者血小板可增高。白细胞及分类多正常。血沉(ESR)和C反应蛋白(CRP)常升高,并且和疾病的活动相关。RA新的抗体不断被发现,其中有些抗体诊断的特异性较RF明显提高,且可在疾病早期出现,如抗CCP抗体。可分为IgM、IgG和IgA型。在常规临床工作中主要检测IgM型RF,它见于约70%的患者血清,其滴度一般与RA的活动性和严重性成比例。但RF并非RA的特异性抗体,其他感染性、自身免疫性疾病及约5%的正常人也可以出现低滴度的RF,RF阴性者也不能排除RA的诊断。有抗核周因子(APF)抗体、抗角蛋白抗体(AKA)、抗聚角蛋白微丝蛋白抗体(AFA)和抗CCP抗体。这组抗体的靶抗原为细胞基质的聚角蛋白微丝蛋白,CCP是该抗原中主要的成分,因此抗CCP抗体在此抗体谱中对RA的诊断敏感性和特异性高,已在临床中普遍使用,并被纳入2010年ACR/EULAR新的RA分类标准评分中。这些抗体有助于RA的早期诊断和鉴别诊断,尤其是血清RF阴性、临床症状不典型的患者。70%的患者血清中出现各种类型的免疫复合物,尤其是活动期和RF阳性患者。在急性期和活动期,患者血清补体均有升高,只有在少数有血管炎者出现低补体血症。正常人关节腔内的滑液不超过3.5ml。在关节有炎症时滑液增多,滑液中的白细胞明显增多,达2000×106/L~75000×106/L,且中性粒细胞占优势,其黏度差,含葡萄糖量低(低于血糖)。其典型的病理改变有助于本病的诊断。
-
+其他辅助检查
其他辅助检查:1. X线平片:对RA诊断、关节病变分期、病变演变的监测均很重要。初诊至少应摄手指及腕关节的X线片,早期可见关节周围软组织肿胀影、关节端骨质疏松(Ⅰ期);进而关节间隙变窄(Ⅱ期);关节面出现虫蚀样改变(Ⅲ期);晚期可见关节半脱位和关节破坏后的纤维性和骨性强直(Ⅳ期)。诊断应有骨侵蚀或肯定的局限性或受累关节近旁明显脱钙。2.超声检查:高频超声能清晰显示关节腔、关节滑膜、滑囊、关节腔积液、关节软骨厚度及形态等,彩色多普勒血流显像(CDFI)和彩色多普勒能量图(CDE)能直观地检测关节组织内血流的分布,反映滑膜增生的情况,并具有很高的敏感性。超声检查还可以动态判断关节积液量的多少和距体表的距离,用以指导关节穿刺及治疗。3.磁共振成像(MRI):MRI在显示关节病变方面优于X线,近年已越来越多地应用到RA的诊断中。MRI可以显示关节炎性反应初期出现的滑膜增厚、骨髓水肿和轻度关节面侵蚀,有益于RA的早期诊断。影像学检查是协助临床医师诊断RA的有效手段。各种影像技术对RA的诊断和疾病监测价值及优劣见表1。EULAR于2013年发布了针对RA选择影像学检查的循证推荐意见,对临床医师正确做出恰当选择有重要的指导作用。应注意,我国RA患者的就医环境与国外差别较大,不同地区影像设备和技术存在差异,临床医师应根据实际情况,恰当选用影像诊断技术以协助确诊。

-
+诊断
诊断:RA的诊断主要依靠临床表现、实验室检查及影像学检查。目前RA的诊断普遍采用美国风湿病学会(ACR)1987年修订的分类标准,见表1。诊断并不困难,但对于不典型及早期RA易出现误诊或漏诊。2010年ACR和欧洲抗风湿病联盟(EULAR)提出了新的RA分类标准和评分系统,见表2,患者按照表中所示标准评分,6分以上可确诊RA,小于6分目前不能确诊RA,但患者有可能在将来满足诊断标准,需密切观察。新标准纳入了炎症标志物ESR、CRP和抗CCP抗体,提高了诊断的敏感性,为早期诊断和早期治疗提供了重要依据,但并不是诊断标准,临床工作中仍应结合不同患者的具体情况,降低误诊率。目前该标准正在临床实践中验证推广。表1 ACR 1987年修订的RA分类标准
1.关节内或周围晨僵持续至少1小时 表2 2010年ACR/EULAR的RA分类标准项目 评分 关节受累情况(0~5分) 1个中到大关节 0分 RF和抗CCP抗体均阴性 0分 CRP和ESR均正常 0分 <6周 0分 - +鉴别诊断
鉴别诊断:RA需与以下疾病进行鉴别。多见于50岁以上者。主要累及膝、脊柱等负重关节。活动时关节痛加重,可有关节肿、积液。手骨关节炎常多影响远端指间关节,尤其在远端指间关节出现赫伯登(Heberden)结节和近端指关节出现布夏尔(Bouchard)结节时有助诊断。大多数患者ESR正常,RF阴性或低滴度阳性。X线示关节边缘呈唇样增生或骨疣形成,如出现关节间隙狭窄多为非对称性。主要侵犯骶髂及脊柱关节,当周围关节受累,特别是以膝、踝、髋关节为首发症状者,需与RA相鉴别。强直性脊柱炎多见于青壮年男性,外周关节受累以非对称性的下肢大关节炎为主,极少累及手关节,骶髂关节炎具典型的X线改变。可有家族史,90%以上患者HLA-B27阳性,血清RF阴性。本病多于银屑病若干年后发生,部分患者表现为对称性多关节炎,与RA相似。但本病累及远端指关节处更明显,且表现为该关节的附着端炎和手指炎。同时可有骶髂关节炎和脊柱炎,血清RF多阴性。部分患者以指关节肿痛为首发症状,也可有RF阳性、ESR和CRP增高,而被误诊为RA。然而本病的关节病变一般为非侵蚀性,且关节外的系统性症状如蝶形红斑、脱发、皮疹、蛋白尿等较突出。血清抗核抗体、抗双链DNA抗体等多种自身抗体阳性。关节炎类疾病有多种,均各自有其原发病特点,在充分了解相关的疾病后鉴别一般不难。- +治疗
治疗:RA关节病变是由炎性细胞浸润及其释放的炎性介质所致。尽早抑制细胞因子的产生及其作用,能有效阻止或减缓关节滑膜及软骨的病变。故RA一经确诊,应及时给予规范治疗。研究显示,不规律使用改善病情抗风湿药(DMARDs)是RA 患者关节功能受限的独立危险因素之一。尽管RA无法根治,但通过达标治疗(treat-to-target)可有效缓解症状和控制病情。达标治疗指治疗达到临床缓解,即28个关节疾病活动度(DAS28)≤2.6,或临床疾病活动指数(CDAI)≤2.8,或简化疾病活动指数(SDAI)≤3.3。在无法达到以上标准时,可以以低疾病活动度作为治疗目标,即DAS28≤3.2或CDAI≤10或SDAI≤11。但应注意,基于评估工具进行疾病活动度的评价也存在一定局限性,有研究显示,关节肿胀的RA患者即使DAS28≤2.6,仍会发生进一步的关节损害。2011年,ACR和EULAR 推出下述缓解标准:压痛关节数、肿胀关节数、C反应蛋白(CRP)水平及患者对疾病的整体评价均≤1,由于其特异度较高,便于评价和记忆,因此已逐渐在临床实践中采用,但其达标率较低,故临床医师可根据实际情况选择恰当的评估标准。对初始治疗的RA患者,考虑到DMARDs起效时间长及不良反应的发生情况,建议每个月监测1次;对确有困难的患者,每3个月监测1次。随机对照试验显示,每个月监测1次并调整用药,相对于每3个月进行1次监测,可进一步降低疾病活动度,延缓放射学进展,提高机体功能和生活质量。随机对照试验显示,中/高疾病活动度患者3 个月内即可出现明显的关节损害进展,建议监测频率为每月1 次。对治疗已达标者,其监测频率可调整为每3~6个月1次。系统评价对现有的63项RA疾病活动度监测与评估工具进行了全面分析,其中对DAS28、SDAI、CDAI三种工具的信度、效度和响应度进行了测量,结果显示DAS28在此三个方面均表现较好。实验室指标,CRP相比红细胞沉降率(ESR)的优势在于对炎症具有更高的敏感度,不易受年龄、性别和类风湿因子(RF)等因素的影响。SDAI、CDAI无需复杂的步骤,公式也更便于记忆。预后不良因素的评估在RA治疗中具有重要意义,能为临床医师调整治疗方案和选择相应药物提供参考。多项预测模型显示,关节疼痛、肿胀数量,以及升高的ESR、CRP、RF 和ACPA 等实验室指标均为关节损害进展的预测因素。预后不良因素可协助医师确定最佳治疗方案。我国一项风湿病注册登记研究显示,RA患者的常见合并症及患病风险依次为心血管疾病(2.2%)、脆性骨折(1.7%)及恶性肿瘤(0.6%),高龄和长病程与其呈正相关。合并此类疾病会影响RA 患者的预后,增加病死率。此外,RA患者也会出现关节外的其他组织和器官受累,研究显示RA 患者关节外受累的发生率为17.8%~47.5%,受累组织和器官包括皮肤、肺、心脏、神经系统、眼、血液和肾脏等,这类RA患者并发症的发生会更多,病死率会更高。因此,临床医师应全面了解患者的病情,合理制订或调整用药方案。传统合成DMARDs是RA治疗的基石,亦是国内外指南共同认可的一线药物。队列研究显示,RA患者诊断第1年内传统合成DMARDs药物的累积使用量越大,关节置换时间越迟;早使用1个月,外科手术的风险相应降低2%~3%[50]。甲氨蝶呤是RA治疗的锚定药。一般情况下,2/3的RA患者单用甲氨蝶呤,或与其他传统合成DMARDs联用,即可达到治疗目标。安全性方面,基于我国人群的研究显示,小剂量甲氨蝶呤(≤10 mg/周)的不良反应轻、长期耐受性较好[52]。此外系统评价显示,甲氨蝶呤治疗期间补充叶酸(剂量可考虑每周5 mg)可减少胃肠道副作用、肝功能损害等不良反应。欧美15个国家的调查显示,甲氨蝶呤平均使用率达到83%,远高于其他药物,但我国甲氨蝶呤的使用率仅为55.9%。鉴于我国医疗卫生经济现状,甲氨蝶呤在我国RA 治疗领域的核心地位和作用应得到进一步巩固和加强。研究显示,对有甲氨蝶呤禁忌者,来氟米特和柳氮磺吡啶单用的疗效和安全性与甲氨蝶呤相当。国际上来氟米特的使用率位于甲氨蝶呤、柳氮磺吡啶、羟氯喹之后,为21%;但在我国的使用率仅次于甲氨蝶呤,为45.9%,在部分地区的使用率甚至超过甲氨蝶呤,应引起临床医师的注意。我国RA患者使用柳氮磺吡啶治疗的安全性较好,但在使用率方面仅为4.4%,远低于国外的43%,且绝大部分为联用其他传统合成DMARDs。柳氮磺吡啶与除甲氨蝶呤外的其他传统合成DMARDs比,根据我国国情,在单药治疗方面更具成本效益比。羟氯喹在我国的使用率为30.4%,国际上的使用率为41%。横断面研究显示,我国羟氯喹的使用以联合用药为主(占95%)。系统评价显示,羟氯喹对RA患者的代谢可能有益,并可能减少心血管事件的发生,故一般情况下,建议将其与其他DMARDs联合使用。经甲氨蝶呤、来氟米特或柳氮磺吡啶等单药规范治疗仍未达标者,建议联合用药。有研究报道,对早期疾病活动度高的RA患者,传统合成DMARDs联合治疗可改善临床症状和关节损害。对甲氨蝶呤反应不足的RA患者,Meta分析显示,联合3种传统合成DMARDs(甲氨蝶呤+柳氮磺吡啶+羟氯喹)能较好地控制疾病活动度,其效果不低于甲氨蝶呤联合一种生物制剂DMARDs 或联合靶向合成DMARDs 。经传统合成DMARDs联合治疗仍不能达标时,可考虑延长治疗时间,观察疗效。多中心随机对照试验显示,对于经传统合成DMARDs积极治疗3~6个月仍不达标的RA患者,延长治疗时间,可进一步提高临床缓解率,且患者用药安全性良好。经传统合成DMARDs治疗未达标的RA患者,建议一种传统合成DMARDs联合一种生物制剂DMARDs,或一种传统合成DMARDs联合一种靶向合成DMARD进行治疗。肿瘤坏死因子α(TNFα)抑制剂是目前证据较为充分、应用较为广泛的治疗RA的生物制剂DMARDs。在北美,生物制剂DMARDs的使用率为50.7%;而我国一项风湿免疫注册登记研究显示,我国生物制剂DMARDs的使用率仅为8.3%。建议对我国符合生物制剂DMARDs适应证的患者应进一步规范化使用。托珠单抗是抗IL-6受体的重组人源化IgG1亚组单克隆抗体,对传统合成DMARDs反应不足的RA患者,建议传统合成DMARDs联合托珠单抗进行治疗。靶向合成DMARDs 是一类具有新作用机制的抗风湿药,目前仅指JAK(Janus kinase)抑制剂。对传统合成DMARDs反应不足的RA患者,可以使用传统合成DMARDs联合JAK抑制剂(托法替布)进行治疗。TNFα抑制剂、托珠单抗和托法替布目前在使用的选择上,并无优先顺序。当传统合成DMARDs联合其中一种治疗未达标后,可在三者间更换另外一种进行治疗。艾拉莫德(iguratimod)是2011年获中国食品药品监督管理总局批准的抗风湿药,其作用机制还有待进一步阐明,目前主要在中国和日本使用。有研究显示,艾拉莫德与甲氨蝶呤联用能改善活动期RA患者的临床症状。此外,2015年APLAR指南提出可使用艾拉莫德治疗活动期RA患者。雷公藤制剂属植物药,自1969年开始用于治疗RA,但由于缺乏安全性和有效性的科学数据,在一定程度上限制了其使用。近2年的研究显示,对无生育要求的RA患者,雷公藤单用或与甲氨蝶呤联用,均具有一定的疗效,且不良反应发生率与单用甲氨蝶呤无显著差异,但在使用过程中需密切监测与评估其毒副作用。此外,如白芍总苷、青藤碱等植物制剂,一方面为RA治疗带来新的可能性,另一方面,尚需开展高质量临床试验来进一步研究其有效性和安全性。糖皮质激素具有高效抗炎和免疫抑制作用,1948年首次用于治疗RA。但由于其副作用较大,因此在较长时间内临床医师很少将糖皮质激素用于治疗RA。系统评价显示,对中/高疾病活动度的RA 患者,在使用传统合成DMARDs的基础上联合小剂量糖皮质激素(泼尼松≤10 mg/d或等效的其他药物)可快速控制症状,协助传统合成DMARDs发挥作用。我国的风湿疾病注册登记研究显示,40.6%的RA患者不同程度地接受过糖皮质激素的治疗。横断面研究显示,糖皮质激素用药不规范问题在我国仍然很突出:用药疗程过长(如大于6个月)的RA患者占70%;仅接受糖皮质激素单药治疗的患者占11.3%。因此糖皮质激素在RA治疗中的使用仍需进一步规范,特别是县级及以下基层医疗机构。基于长期使用生物制剂DMARDs或靶向合成DMARDs的安全性,以及我国RA患者使用上述两类药物的经济承受力,在治疗达标后开始对其进行逐渐减量,这在我国RA治疗策略中具有重要意义。系统评价显示,一般经生物制剂DMARDs或靶向合成DMARDs 治疗6个月左右可达标;达标后生物制剂DMARDs减量的复发率低于直接停药者,与不减量者的复发率相当;有1/3~1/2的RA患者在停药后1年内仍处于临床缓解或低疾病活动度;停用靶向合成DMARDs 者的疾病活动度总体高于非停药者,但同时有37%的患者停药后1年内未复发。如果RA患者处于持续临床缓解状态1年以上,临床医师可根据患者病情、用药情况,以及患者的经济状况等,与患者讨论是否停用生物制剂DMARDs或靶向合成DMARDs。患者教育对疾病的管理至关重要,有助于提高RA的治疗效果。一方面,临床医师应帮助患者充分了解和认识RA的疾病特点与转归,增强其接受规范诊疗的信心,并提醒患者定期监测与随访;另一方面,建议RA患者注意生活方式的调整。肥胖和吸烟不仅增加RA的发病率,也会加重RA的病情。研究显示,合理饮食有助于RA患者的病情控制。每周坚持1~2次的有氧运动(而非高强度的体育运动),不仅有助于改善患者的关节功能和提高生活质量,还有助于缓解疲劳感。类风湿关节炎的诊疗流程(图1)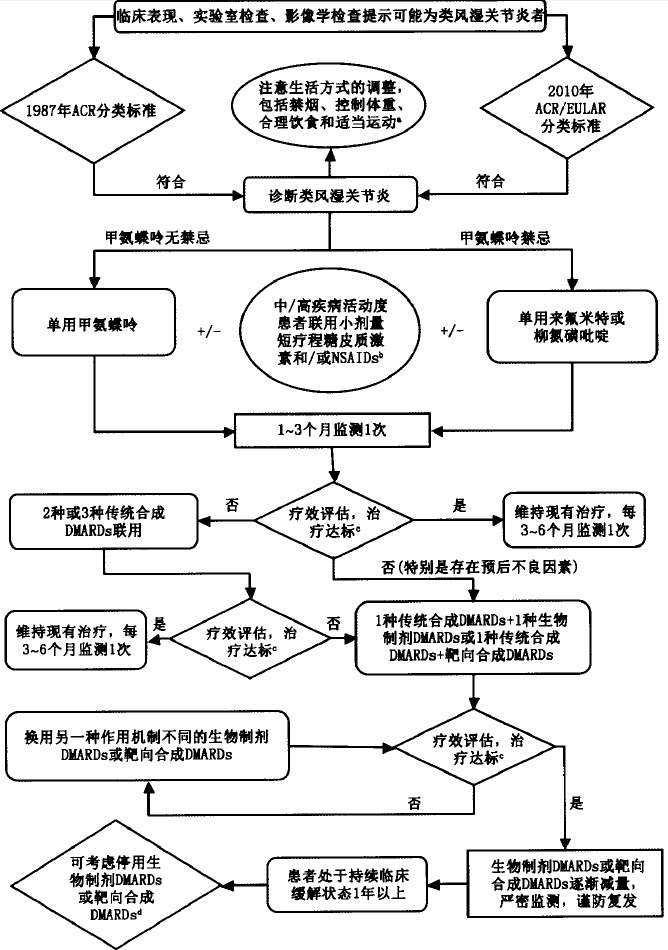

- +预后
机构解读
- +鉴别诊断
